Le chapitre :
Le cours du chapitre 6
Comment expliquer la polarité d’une entité à partir de sa structure ?
Électronégativité des atomes, évolution dans le tableau périodique.
Polarisation d’une liaison covalente, polarité d’une entité moléculaire.
•Déterminer le caractère polaire d’une liaison à partir de la donnée de l’électronégativité des atomes.
•Déterminer le caractère polaire ou apolaire d’une entité moléculaire à partir de sa géométrie et de la polarité de ses liaisons.
Les prérequis du chapitre :
Rappel de seconde ... qui ne sont pas des rappels cette année !
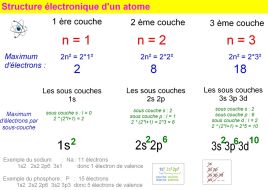
Analyse de configuration électronique, électrons de valence, stabilité des gaz nobles, ions monoatomiques, modèle de la liaison covalente, lecture de schémas de Lewis de molécules
Schéma de Lewis d’une molécule, d’un ion mono ou polyatomique.
Lacune électronique.
Géométrie des entités.
•Établir le schéma de Lewis de molécules et d’ions mono ou polyatomiques, à partir du tableau périodique : O2,H2, N2,H2O, CO2,NH3,CH4,HCl, H+,H3O+,Na+,NH4+,Cl-,OH-, O2- .
•Interpréter la géométrie d’une entité à partir de son schéma de Lewis.
•Utiliser des modèles moléculaires ou des logiciels de représentation moléculaire pour visualiser la géométrie d’une entité.
Site de Physique - Chimie de GROSSHENY Laurent
Site de Physique - Chimie de GROSSHENY Laurent